非劣效性与等效性试验的CONSORT声明 |
您所在的位置:网站首页 › Consort声明 官网 › 非劣效性与等效性试验的CONSORT声明 |
非劣效性与等效性试验的CONSORT声明
|
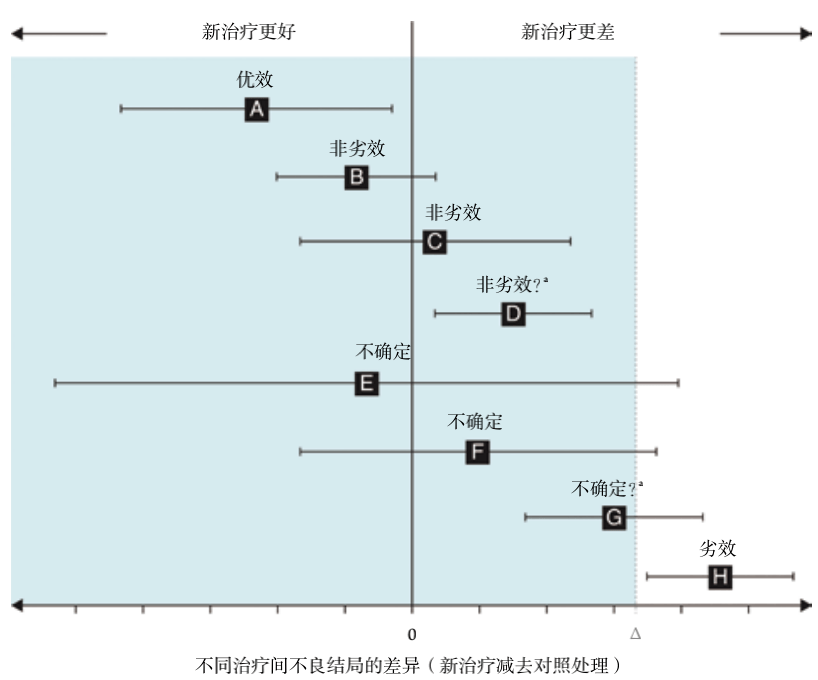
三、何时使用该报告指南(涵盖哪些类型的研究) 非劣效性与等效性试验的CONSORT声明可用于报告非劣效性和等效性随机试验(如前所述)。非劣效性试验旨在确定一种新的治疗方法是否在一个可接受的范围内不劣于主动对照的治疗方法。由于不可能证明完全相同,因此为主要患者结局的治疗效果定义了预先设定的非劣效性界限(Δ)(图14-1)。等效性试验与之非常相似,只是等效性定义为治疗效果介于−Δ和+Δ之间。新的治疗方法通常有一个或多个优点,例如副作用少、给药更方便、成本更低、侵入性更小或在其他方面更方便。
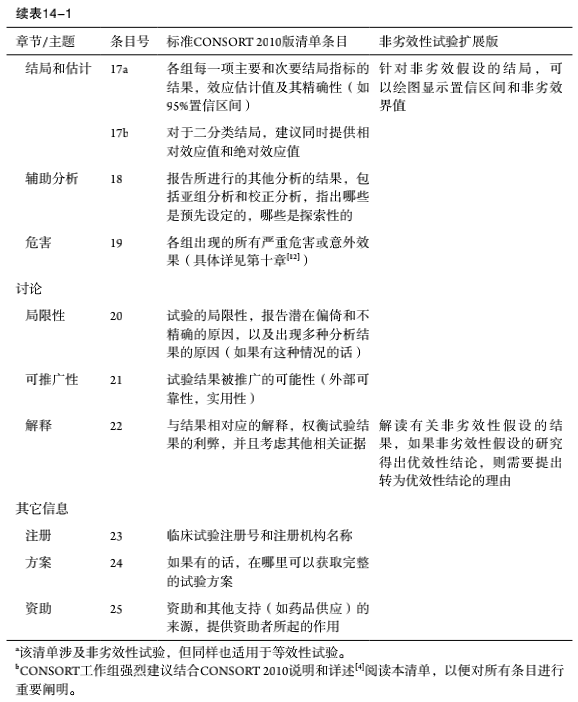
图14-1(经 JAMA 许可复制),误差线表示双侧95%置信区间(Confidence Intervals,CI) x=Δ处的虚线表示非劣效性界值;x=Δ左侧的区域表示非劣效性区域。A:如果CI完全位于零的左侧,则新的治疗方法更优。B和C:如果CI位于Δ左侧且包含零,则新的治疗方法是非劣效的,但未显示出优效性。D:如果CI完全位于Δ的左侧,并且完全位于零的右侧,因此可以认为非劣效,但是和标准治疗相比,新治疗又明显更差,这种令人费解的情况是罕见的,往往需要非常大的样本量。E和F:如果CI包括Δ和零,则差异不显著,但关于非劣效性的结果不确定。G:如果CI包括Δ并且完全在零的右侧,则差异在统计上是显著的,但对于等值或更差的Δ的可能劣性,结果则不确定。H:如果CI完全高于Δ,则新的治疗方法较差。a该置信区间表示不包括Δ的非劣效性,但新的治疗明显比标准治疗差。这样的结果不太可能,因为它需要非常大的样本量。b该置信区间是不确定的,因为真实的治疗差异小于Δ仍然是可信的,但是新的治疗明显比标准治疗差。 四、 当前/历史 版本 当前版本与2006年原始CONSORT非劣效性和等效性试验的扩展版有以下不同: (1)在单独的列中呈现CONSORT的标准清单条目和非劣效性试验的扩展版条目(表14-1和表14-2)。 (2)提供了非劣效性随机对照试验摘要的扩增和条目。 (3)更新了报告良好的实例。 (4)更新关于非劣效性试验的常见程度和试验报告质量的章节。 (5)纳入了最近方法学发展的总结。
五、扩展和(或)实施 非劣效性与等效性试验的CONSORT声明本身就是经典CONSORT声明的扩展版。没有其他非劣效性和等效性试验的报告指南。 六、相关动态 非劣效性试验激增,是因为人们希望引入比标准药物更具优势的新药,例如副作用少、成本更低、侵入性更小或更方便的药物。许多国家的监管机构正在制订非劣效性试验的指南。特别是美国食品和药品管理局最近发布了更新的指南[7] 。 七、如何有效使用本指南 第九章解释如何最好地使用CONSORT主清单。在投稿过程中,编辑可以要求作者填写《非劣效性与等效性试验的CONSORT声明清单》,连同稿件一并提交,同时也可以参考已发表的非劣效性和等效性CONSORT声明文章。编辑可以要求同行评议者使用相同的清单来指导他们的同行评议过程。 开展非劣效性或等效性试验的研究人员,除了在报告前,还可以在非劣效性或等效性试验开始之前,参考非劣效性与等效性试验的CONSORT声明,了解此类试验的设计、实施和分析的一般问题。 读者可能会发现,该指南有助于指导他们对已发表的非劣效性和等效性试验报告进行批判性评价。 八、研发过程 见前文提到的历史与发展。 九、报告指南的有效性 我们尚不清楚使用CONSORT非劣效性和等效性扩展版清单和(或)流程图是否与非劣效性和等效性试验报告质量的提高有关。 十、认可和遵守 在支持CONSORT声明的同时,期刊也间接地认可了它的扩展版。编辑们应该意识到,非劣效性和等效性扩展版的清单中有针对这些试验的附加条目。 十一 、注意事项和局限性(包括范围) 一般CONSORT声明的所有注意事项和局限性均适用于本报告指南。与一般CONSORT声明一样,本报告指南要求报告的完整性、清晰性和透明度,这应反映实际的试验设计和实施。在非劣效性和等效性试验中,设计中的缺陷,例如非劣效性或等效性的界值过大,可能导致使用稍差的治疗(“生物爬行现象”)。试验实施过程中的缺陷可能会使新治疗和标准治疗之间的差异在任何一个方向上产生偏差,从而导致采用劣效治疗或不采用非劣效治疗的风险。 十二、错误和误解 非劣效性和等效性试验有许多共同点,但并不相同:非劣效性试验旨在证明一种新的治疗方法不会比标准治疗方法差一点(非劣效性界值)。大多数非优效性试验的治疗性和预防性试验解决的是非劣效性问题,而不是等效性问题。双侧等效性试验的目的是证明两种治疗方法或组合在特定范围内结果相似,它们在生物等效性评估中更为常见。 从优效性到非劣效的转换:优效性试验中不显著的结果并不意味着非劣效或等效。一些优效性试验在未能显示出优效性结果的情况下,报告结果就像非劣效性试验或等效性试验一样[11-12] 。 非劣效性或等效性界值(Δ)的选择:有时Δ太大,这增加了接受非劣效治疗为非劣效性治疗的可能性[13] ,这对死亡率等主要结果来说是特别值得关注的。 检测灵敏度和恒定性假设:新疗法相对于标准疗法显示出非劣效性并不能保证新疗法有效。确保非劣效性试验检测敏感性的方法是在试验中同时加入安慰剂对照组和主动对照组(标准治疗),若已知标准治疗有效,出于伦理学原因,这通常是不可能的。非劣效性试验假设主动对照组和安慰剂组之间的历史差异在目前是有效的。随着医疗实践和护理标准的快速变化,情况可能并非如此[14-15] 。 非劣效性假设不需要计算单侧置信区间:即使为了显示非劣效性(单侧等效),也建议使用具有适当预设显著性水平的双侧置信区间。如果观察到的效果与预期相反,也允许评估新治疗的优效性,但这不能用单侧置信区间来完成[1,7,12] 。 十三、制定者的首推内容 该报告指南的优先关注点是指与非劣效性和等效性试验结果的目的、分析和解释相关的问题,这些问题在文献中经常被不充分地陈述或报道。 目的:非劣效性试验旨在显示一种新疗法的疗效是否至少与标准疗法相当,或比标准疗法差的量是否小于Δ。 分析:排除未接受指定治疗或不遵守方案的患者的分析可能会使试验偏向任何一个方向。意向性治疗(intention-to-treat,ITT)(或治疗中)和按研究方案(per-protocol,PP)分析这两个术语经常被使用,但定义可能不充分[4] 。在优效性试验中,潜在的非ITT偏倚分析不如ITT理想,但仍然可以提供一些有用信息。在非劣效性和等效性试验中,非ITT分析可能是可取的,因为ITT增加了错误得出非劣效性结论的风险。 解释:除非与预先确定的非劣效性界值明确相关,否则在优效性试验事后声称非劣效性是不合适的。 解释:图14-1显示了非劣效性试验中观察到的不良结果的治疗差异的可能情况。 十四、未来规划 若有新的重要研究发现或随机平行对照试验的CONSORT声明有进一步更新,CONSORT小组将更新本报告指南。 参考文献(向上滑动阅读) [1] Piaggio,G.,Elbourne,D.R.,Altman,D.G. et al. (2006) Reporting of noninferiority and equivalence randomized trials:an extension of the CONSORT statement. JAMA,295,1152-1160. [3] Schulz,K.F.,Altman,D.G. & Moher,D. (2010) CONSORT 2010 statement:updated guidelines for reporting parallel group randomised trials. BMJ,340,c332. [4] Moher,D.,Hopewell,S.,Schulz,K.F. et al. (2010) CONSORT 2010 Explanation and Elaboration:updated guidelines for reporting parallel group randomised trials. BMJ,340,c869. [5] Hopewell,S.,Clarke,M.,Moher,D. et al. (2008) CONSORT for reporting randomised trials in journal and conference abstracts. Lancet,371,281-283. [6] Hopewell,S.,Clarke,M.,Moher,D. et al. (2008) CONSORT for reporting randomized controlled trials in journal and conference abstracts:explanation and elaboration. PLoS Medicine,5 (1),e20. [7] Moher,D.,Schulz,K.F. & Altman,D. (2001) The CONSORT Statement:revised recommendations for improving the quality of reports of parallel-group randomized trials. JAMA,285 (15),1987-1991. [8] Begg,C.,Cho,M.,Eastwood,S. et al. (1996) Improving the quality of reporting of randomized controlled trials. The CONSORT statement. JAMA,276 (8),637-639. [9] FDA (March 2010) Guidance for Industry. Non-Inferiority Trials. [10] Ioannidis,J.P.,Evans,S.J.,Gotzsche,P.C. et al. (2004) Better reporting of harms in randomized trials:an extension of the CONSORT statement. Annals of Internal Medicine,141 (10),781-788. [11] Le Henanff,A.,Giraudeau,B.,Baron,G. & Ravaud,P. (2006) Quality of reporting of noninferiority and equivalence randomized trials. JAMA,295,1147-1151. [12] Boutron,I.,Dutton,S.,Ravaud,P. & Altman,D.G. (2010) Reporting and interpretation of randomized controlled trials with statistically nonsignificant results for primary outcomes. JAMA,303,2058-2064. [13] Gøtzsche,P.C. (2006) Lessons from and cautions about noninferiority and equivalence randomized trials. JAMA,295,1172-1174. [14] D’Agostino,R.B. Sr.,Massaro,J.M. & Sullivan,L.M. (2003) Non-inferiority trials:design concepts and issues-the encounters of academic consultants in statistics. Statistics in Medicine,22,169-186. [15] Kaul,S. & Diamond,G.A. (2006) Good enough:a primer on the analysis and interpretation of noninferiority trials. Annals of Internal Medicine,145,62-69. 译者: 孙艳武
孙艳武, 福建医科大学附属协和医院结直肠外科。外科学博士,副主任医师。从事结直肠癌的微创外科治疗及基础研究。参编学术专著2部,主持省部级课题1项和厅级课题2项。以第一作者发表SCI论文及中文核心期刊论文20余篇。现为《中国普通外科杂志》中青年编委(2019年及2020年度 “最佳审稿专家”)。 审校者:罗旭飞
罗旭飞, 兰州大学公共卫生学院/兰州大学基础医学院循证医学中心公共卫生硕士研究生。主要研究方向为循证公共卫生决策,参与中华医学会多个分会牵头的20余部循证指南制订和评审,发表相关研究论文60余篇,其中SCI收录30余篇,担任第一届国家免疫规划技术工作组成员。 审校者: 张先卓
张先卓, 兰州大学第一临床医学院/兰州大学基础医学院循证医学中心。普外科硕士在读,湖北恩施人。学习循证医学、基础研究、临床研究、大数据及生信相关研究,发表中英文论文若干篇、审校和翻译专著几本。疫情期间参与多项相关研究和志愿工作。坚信:知识、汗水、灵感、机遇。 资讯 AME旗下13本期刊最新影响因子|2021年6月 责任编辑:陈 童 AME Publishing Company 排版编辑:袁 舒 AME Publishing Company b.01. 20 21. 10.21.02 点击 阅读原文 了解AME返回搜狐,查看更多 |
【本文地址】
今日新闻 |
点击排行 |
|
推荐新闻 |
图片新闻 |
|
专题文章 |